生物学试验与评价
 生物学试验与评价
生物学试验与评价
有接触风险的医疗器械均需要开展生物学试验与评价。
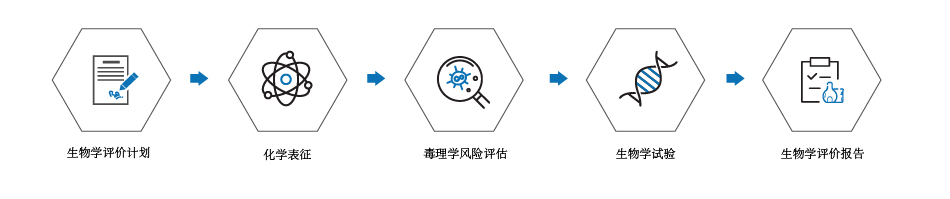
医疗器械生物学评价程序应当按GB/T 16886.1-ISO 10993.1给出的评价流程图开展;生物学试验应当由有生物学试验资质的机构按GB/T 16886-ISO 10993系列标准规定进行并出具报告。
微谱医疗器械团队为企业提供完整的生物学试验与评价服务。
评价流程图:
 服务项目
服务项目
01、生物学试验
(1)体内测试
刺激试验:皮内反应、皮肤敷贴、阴道刺激、直肠刺激、口腔黏膜刺激;测试系统:兔,金黄地鼠
热原试验:中国药典、美国药典;测试系统:兔
植入试验:皮下植入、肌肉植入、骨植入;测试系统:兔,大鼠
全身毒性试验:急性、亚急性、亚慢性、慢性;测试系统:大/小鼠,兔
致敏试验:豚鼠最大致敏、封闭敷贴法;测试系统:豚鼠
血栓形成试验:测试系统:比格犬
(2)体外测试
细胞毒性:浸提液试验(MTT试验)、直接接触试验和间接接触试验(琼脂扩散试验和滤膜扩散试验)。
遗传毒性:染色体畸变试验、细菌回复突变试验、小鼠淋巴瘤试验、微核试验血液相容性:溶血、补体激活、部分凝血酶时间测定、白细胞和血小板计数试验
02、毒理学风险评估
医疗器械毒理学风险评估应当按GB/T 16886.17-ISO 10993.17开展;毒理学风险评估是为了对医疗器械中每种化学物质(材料、预期的添加剂、加工过程污染物和残留物、可沥滤物、降解产物等)进行评估(建立每日允许暴露量PDE/允许限量AL和安全边际值MOS),并确定是否需要进一步测试或分析以降低风险。
03、生物学评价报告
生物学评价专家汇总确定下述内容并最终形成《生物学评价报告》,得出医疗器械生物学安全性的结论。内容包括但不限于:
(1)医疗器械生物学评价的策略和所含程序;
(2)医疗器械所用材料选择的描述;
(3)材料表征
●-医疗器械材料的定性与定量的说明或分析
●-医疗器械材料与市售产品的等同性比较
(4)选择或放弃生物学试验的理由和论证;
(5)已有数据和试验结果的汇总;
(6)完成生物学评价所需的其他数据。
04、药代与毒代动力学研究
医疗器械药代与毒代动力学研究应当按《化学药物非临床药代动力学研究技术指导原则》和GB/T 16886.16-ISO 10993.16开展; 药械组合器械和可吸收器械需考虑开展药代与毒代动力学研究。
 服务优势
服务优势
01. 国家CMA和CNAS资质实验室
02. 行业认可的、经验丰富的生物学评价团队
03. 中美资质认证的、经验丰富的毒理学专家团队
 服务案例
服务案例
服务器械包含所有二、三类器械,服务产品包含心血管植介入器械、骨科植入物、输注器具、血液净化器械、药械组合产品等。
典型案例
|
产品名称 |
骨科植入—3D打印椎间融合器(常见材料钛合金TC4) |
|
|
接触分类 |
植入器械,组织/骨(>30d) |
|
|
考虑的生物学评价终点 |
需开展的生物学试验 |
MTT细胞毒性试验 |
|
皮肤致敏试验-最大剂量法 |
||
|
皮内反应试验- |
||
|
热原试验 |
||
|
急性全身毒性试验 |
||
|
细菌回复突变试验 |
||
|
染色体畸变试验 |
||
|
骨植入试验- |
||
|
亚急性全身毒性 |
||
|
亚慢性全身毒性 |
||
|
可考虑豁免的生物学试验终点 |
慢性全身毒性 |
|
|
致癌性 |
||
|
材料表征/可沥滤物分析/毒理学评估 |
产品组分成分分析-材料鉴定 |
|
|
工艺验证:清洁验证ISO 19227(TOC、THC等) |
||
|
性能验证:耐腐蚀性、金属离子析出(Ti、Al、V、Fe) |
||
|
可浸提物/可沥滤物分析/毒理学风险评估豁免慢性和致癌性,建议进行等同性比较方式开展试验 |
||
|
包材生物学评价 |
红外光谱、蒸发残渣、微粒、细胞毒性 |
|
 平台能力/相关仪器设备
平台能力/相关仪器设备
01. 大鼠、小鼠、豚鼠、金黄地鼠、兔




02. 病理临检设备